白内障(专业版)
白内障是眼睛的晶状体出现混浊,导致视力下降。它与增龄老化、遗传、营养障碍、免疫与代谢异常和辐射等有关,导致晶状体蛋白质变性而发生混浊,称为白内障。
定义
白内障是眼睛的晶状体出现混浊,导致视力下降。它与增龄老化、遗传、营养障碍、免疫与代谢异常和辐射等有关,导致晶状体蛋白质变性而发生混浊,称为白内障。眼睛的晶状体将图像聚焦在眼睛后部的视网膜上,它是处理图像的地方,然后发送到大脑。随着白内障的成熟,它经常会引起眩光,以及视力下降。如果白内障开始变黄,对颜色敏感度也可能会下降。
病因
眼睛的晶状体主要由水和蛋白质组成。蛋白质的排列方式使晶状体保持清晰,以便光线可以通过它。当一些蛋白质聚集在一起并开始对晶状体形成云状时,就出现白内障了。白内障不会从一只眼睛扩散到另一只眼睛,尽管大多数人在同一时间双眼都会出现白内障。长期的氧化应激和糖基化是白内障形成的主要病理过程。来自线粒体的自由基损害细胞结构,包括蛋白大分子以及DNA等,使细胞功能紊乱。眼内上皮细胞对氧化应激特别敏感,而这层细胞氧化损伤可导致晶状体混浊逐渐形成。蛋白质糖基化与糖尿病、年龄老化和肾功能衰竭等密切相关,晶状体蛋白易受到糖基化影响,逐渐形成所谓的蛋白糖基化终产物(AGEs),促成白内障形成。
白内障有以下几种诱因,包括:
- 年龄老化,最常见的原因
- 吸烟
- 糖尿病
- 某些感染
- 暴露于辐射、某些毒素或药物
- 长时间服用肾上腺皮质激素
- 出生缺陷,先天性代谢缺陷,或染色体异常
风险因素
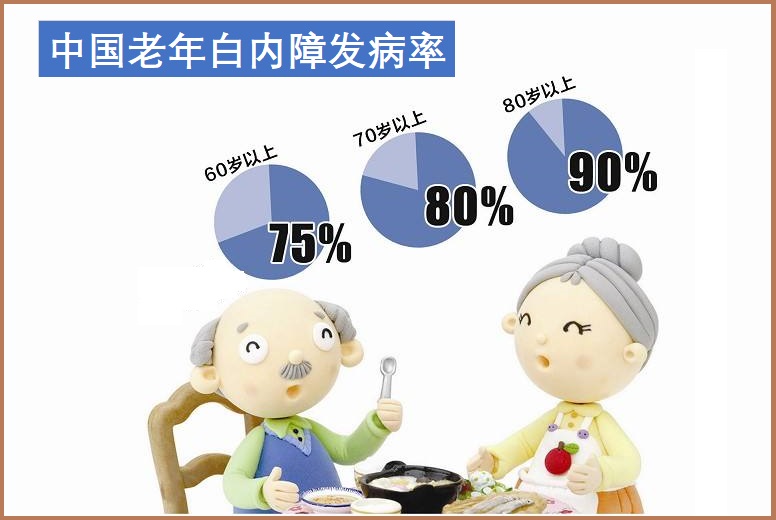
年龄老化是主要风险因素,一般在40岁以上即可出现,年龄越大、发病率越高。其他可能增加白内障机率的因素包括:
- 过度暴露于阳光下紫外线辐射
- 营养不良或失衡
- 家庭成员患白内障
- 糖尿病
- 高血压
- 甲状旁腺功能减退症
- 眼睛创伤
- 慢性眼病,如葡萄膜炎或色素性视网膜炎
- 吸烟
- 经常饮酒过量
- 自体免疫疾病,如类风湿性关节炎等
- 长期使用类固醇药(糖皮质激素)
症状
当白内障处于早期阶段,可能不会注意到视力有任何变化。白内障往往慢慢地成熟,视力逐渐恶化。一些患有白内障的人发现他们的近距离视力突然提高了,但这只是暂时的。随着白内障出现,视觉可能恶化。由于视力下降是渐进的,许多人在常规眼科检查之前没有发现白内障。
白内障可能引起如下症状:
- 浑浊或视力模糊
- 颜色似乎褪色或图像出现一个黄色的色调
- 对比度差
- 夜间视力差
- 阅读困难
- 双重或多重视觉症状
- 增加近视,需要频繁改变佩戴的眼镜
- 对光线出现问题,包括如下:
- 在晚上看灯觉得特别亮
- 耀眼的灯光或耀眼的阳光
- 灯光围绕的光环
- 试图在明亮的灯光下读书
- 从黑暗处移动到明亮处时的问题
- 颜色似乎变淡或消失了
- 夜间视力差
- 在罕见的病例中,白内障可能引起急性青光眼发作。
疗法
综合疗法可包括如下:调整饮食与生活方式
- 饮食富含新鲜蔬菜、水果,有助于预防白内障。
- 减少红肉(猪牛肉等),适当增加鱼肉尤其是深海鱼摄入。
- 不抽烟或戒烟,长期吸烟对眼睛损害大。
- 适度饮酒,不宜过量。
- 注意休息、防止眼疲劳。
- 坚持运动锻炼。
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控白内障营养和草本补充剂,主要包括如下:
一、抗氧化保护
1.谷胱甘肽:
由于谷胱甘肽在晶状体中的浓度非常高,并且对晶状体透明度至关重要,因此它是晶状体中重要的内源性抗氧化分子1。谷胱甘肽直接清除活性氧和自由基,防止晶状体中结构蛋白的氧化;这在几种类型的白内障中尤为重要,其中晶状体蛋白的氧化损伤似乎起着关键作用2,3。在清除活性氧和自由基后,谷胱甘肽的氧化形式很容易被一种特殊的酶回收4。
随着年龄的增长,谷胱甘肽的循环逐渐减少,还原型谷胱甘肽储备减少,氧化型谷胱甘肽开始积累5。在被称为晶状体核的成人晶状体中心尤其如此,即使少量的紫外线照射也会导致自由基的形成和白内障的产生1,6。这些营养素如N-乙酰半胱氨酸、硫辛酸、褪黑素和硒等,可自然增加体内谷胱甘肽的合成和活性7-9。
2.维生素C:
维生素C通过充当ROS和自由基的“池子”,在晶状体中提供额外的抗氧化支持。其氧化形式,脱氢抗坏血酸,随后被谷胱甘肽转化回抗坏血酸,并间接地依赖谷胱甘肽的反应1,4,10。因此,维生素C和谷胱甘肽被认为可以共同促进晶状体内的适当水分平衡,防止蛋白质结块。
晶状体中维生素C的浓度是血浆中维生素C浓度的20-30倍,这一发现支持了维生素C对眼睛健康的重要性11。此外,它的重要性得到了实验的支持,实验表明,回收谷胱甘肽的酶的抑制剂会导致脱氢抗坏血酸的显著增加,如果脱氢抗坏血酸不能转化回维生素C,则会导致动物晶状体透明度的丧失1,10。
一项针对女性长期饮食补充维生素C效果的研究表明,10年以上的补充可以显著降低晶状体任何部位早期年龄相关性白内障的发病率。重要的是,这项研究排除了以前被诊断为白内障的女性,以确保那些在医生的建议下开始补充维生素C并因其诊断而补充维生素C的女性不包括在内12。另一项包括大量男性和女性的研究表明,大量摄入维生素C,单独或与其他抗氧化剂(维生素E、β-胡萝卜素和锌)一起,可以预防核白内障的发展13。一项招募了4000多名参与者的研究报告称,血清中维生素C每增加1mg/dL,白内障的发病率就会下降26%14。此外,在印度的一项研究中,共有5600多人参与,发现血清维生素C水平高与白内障发病率低之间存在密切联系11。
3.维生素B2:
维生素B2(又称核黄素)是黄素腺嘌呤二核苷酸(FAD)的重要成分。FAD直接参与分解碳水化合物和脂质,对适当的细胞能量平衡很重要,也被将谷胱甘肽回收回其生物活性形式的酶所使用。在几种动物模型中表明,缺乏膳食核黄素会导致白内障15。
几项针对人类的研究表明,核黄素在预防白内障形成方面很重要。在一项研究中,饮食中核黄素摄入量最高的女性与摄入量最低的女性相比,患白内障的风险较低16。另一项研究报告称,饮食中核黄素摄入量最高的人患白内障的风险降低了约50%17。
4. N-乙酰半胱氨酸(NAC):
NAC是一种强大的抗氧化剂和半胱氨酸的衍生物,已被证明可以防止晶状体混浊18。NAC还支持谷胱甘肽的合成19-21。通过将NAC与大蒜油中的一种主要有机硫化物二烯丙基二硫醚结合,研究人员发现后者可以增强NAC的抗氧化性能,这种结合可以防止白内障的形成22。在动物模型中,NAC已被证明可以预防晶状体混浊和抑制白内障形成18,23。另一项研究发现,NAC和谷胱甘肽乙酯(GS-EE)的组合,作为滴眼液,在大鼠早期阶段轻微抑制糖尿病白内障的进展24。
5.硫辛酸:
有证据表明,强效抗氧化剂硫辛酸可能有助于预防糖尿病性白内障的形成25-27。由于硫辛酸分布在细胞和组织的脂溶性和水溶性区域,它能中和各种自由基25,28。硫辛酸有两种形式:R-硫辛酸和S-硫辛酸。在这两者中,分离的R-硫辛酸被证明可以预防白内障的形成26。与作为两种形式的混合物的α-硫辛酸相比,R-硫辛酸的更高功效可能与晶状体对R-硫辛酸吸收的更高速率有关。
6.维生素E:
维生素E天然存在于8种不同的化学形式中,包括α-生育酚和γ-生育酚29,30。它具有独特的抗氧化特性,防止脂肪酸分解过程中产生的自由基积累。由于维生素E是脂溶性的,它通过中和自由基和ROS来保护脂肪组织和细胞膜。
一项针对女性的研究表明,那些从食物和补充剂中摄入维生素E最多的人患白内障的风险降低了14%31。另一项针对40-79岁参与者的研究显示,维生素E水平较低的人更容易出现晶状体混浊32。另一项研究表明,总生育酚水平(血清α-生育酚和γ-生育酚的总和)与患白内障的风险降低有关33。
7.褪黑素:
褪黑素是一种天然存在的激素,已被证明可以减少晶状体中的氧化应激,并防止白内障的形成34,35。尽管所涉及的机制尚未确定,但谷胱甘肽产量的增加或自由基的直接清除被认为与此有关36。鉴于褪黑激素水平随着年龄的增长而下降,并且考虑到晚年白内障发病率的上升,补充褪黑激素可能有助于老年人预防白内障36。
二、支持眼健康:
1.类胡萝卜素:
类胡萝卜素是一种存在于植物中的色素,可以吸收光线并防止紫外线的氧化作用。包括叶黄素、玉米黄质和消旋玉米黄素在内的几种类胡萝卜素不仅在视网膜中高水平存在,而且有助于预防白内障形成和黄斑变性37-39。
一项针对45-71岁女性的研究表明,饮食中的叶黄素和玉米黄质以及富含这些类胡萝卜素的食物可以降低白内障的风险,这些白内障严重到需要手术治疗40。另一项针对40岁以上人群的大型研究发现,饮食中摄入大量叶黄素和玉米黄质的人患核白内障的风险较低41。在一项针对1802名女性的研究中,与最低五分之一的女性相比,血液水平或饮食中叶黄素和玉米黄质摄入量最高五分之一的受试者患核白内障的可能性低32%42。在另一项针对17名白内障患者的小型双盲随机临床试验中,补充叶黄素(15mg,每周3次,持续2年)与改善视力有关43。
2.越橘:
越橘富含花青素(一种植物色素),可在人体内发挥多种有益作用,包括作为抗氧化剂和调节炎症过程44,45。重要的是,在动物模型眼睛中,观察到了这些抗炎和抗氧化作用46。在一个涉及易患老年性眼病(如黄斑变性和白内障)的动物的实验模型中,长期服用越橘提取物完全消除了晶状体和视网膜的损伤,而70%的对照动物患上了白内障和黄斑变性47。
越橘尚未在大型试验中进行研究,以评估其对人类白内障的影响。但对照研究发现,单独或与其他支持眼睛健康的营养素联合补充越橘,对眼睛疲劳和青光眼有好处48,49。
3.硒:
硒是一种微量矿物质,参与人体内的许多生物功能。研究表明,硒可以通过降低晶状体中的氧化应激来减缓白内障的发展50。尽管还需要更多的研究来确定硒如何防止晶状体中的氧化损伤,但它已被证明可以增强谷胱甘肽再循环51,52。
4.维生素K:
维生素K是一种脂溶性维生素,存在于菠菜和羽衣甘蓝等绿叶蔬菜中。维生素K1或叶绿醌是饮食中维生素K的主要来源53。维生素K1已被证明能抑制醛糖还原酶,醛糖还原酶将葡萄糖转化为山梨醇。山梨醇在晶状体中的积累有助于白内障的发病机制54,55。防止山梨醇及其降解产物(果糖)在晶状体中的积累可以降低自由基应激并减少渗透压,降低白内障形成的风险55,56。
一项大型随机对照试验的回顾性分析发现,饮食中维生素K1摄入越多,白内障风险越低。该试验招募了5860名地中海人,并通过食物问卷评估了饮食中维生素K1的摄入量。经过近六年的随访,摄入最高水平维生素K1的参与者患白内障的风险比摄入最低水平的参与者低29%57。
二、抗糖化反应,保护晶状体结构和功能
1.肌肽:
肌肽及其衍生物N-乙酰基肌苷是糖基化反应和氧化损伤的有效抑制剂;它已被证明有效地穿透晶状体58-60。与谷胱甘肽一样,肌肽水平随着年龄的增长而降低61,62。在中等高浓度下,肌肽能够减弱紫外线诱导的晶状体蛋白聚集63。当每天2次以滴眼液的形式局部给药时,N-乙酰肌肽已被证明可以延缓糖尿病诱导的白内障的发作64,65。
N-乙酰肌肽碱滴眼液也被证明对狗有效。据报道,80%的参与犬使用含有N-乙酰基-卡诺西碱的滴眼液后视力得到改善66。结合来自人类试验和啮齿类动物实验的信息,N-乙酰肌肽滴眼液似乎可以对白内障的形成和发展提供相当大的保护64-67。
2.乙酰L肉碱:
肉碱是一种存在于所有哺乳动物中的氨基酸类化合物,对细胞能量来源的线粒体正常功能起着重要作用;其衍生物乙酰L肉碱是一种强大的抗氧化剂,已被证明可以对抗糖基化反应68-70。
对提取的人类白内障晶状体的检查表明,随着混浊程度的增加,肉碱浓度降低,其中混浊程度最高的晶状体的肉碱浓度比混浊程度最低的晶状体低约30%71。在白内障动物模型中,乙酰L肉碱强烈抑制化学诱导的白内障形成。研究人员将乙酰-L-肉碱的作用归因于其在晶状体中作为抗氧化剂的作用72。在随后的一项研究中,同一小组的研究人员表明,乙酰L肉碱也可以防止晶状体细胞的“自我毁灭”或凋亡73。也有证据表明,乙酰L肉碱通过上调内在抗氧化防御机制,防止电离辐射暴露后白内障的发生74。
3.维生素B6:
维生素B6(吡哆醇)是氨基酸代谢和DNA复制和修复所需核酸合成所必需的重要水溶性辅因子。已经证明它显著降低糖尿病晶状体中AGEs的产生75,76。尽管仍需对白内障患者进行人体研究,但一项对糖尿病患者服用维生素B6和维生素B1的试验表明,该组合显著抑制了白细胞中的DNA糖基化,表明对全身有益77。
4.槲皮素:
生物类黄酮是一类具有抗氧化特性的植物衍生分子,它可能有助于对抗晶状体细胞内的水分积聚而破坏正常的光折射,因此对白内障有益78,79。具体而言,槲皮素是人类饮食中摄入最广泛的类黄酮,它被证明可以抑制糖尿病白内障的发展,可能通过多种途径发挥作用,并在氧化应激时保持晶状体的透明度80,81。另一项动物实验表明,槲皮素通过平衡晶状体内的钙、钠和钾离子,有助于保持晶状体透明度82。
更多内容可点击其个性化综合干预方案如下:
- 白内障防控要略(防晶状体病变)
- 白内障防控要略(抗高血糖白内障)
- 白内障防控要略(保护视力)
- 白内障防控(40-55岁)
- 白内障防控(56-65岁)
- 白内障防控(66-75岁)
- 白内障防控(76岁以上)
以及参阅本网如下专文了解有关内容:
医疗干预
白内障的治疗主要依靠手术。
- 白内障手术需要等待,直到患者病情进展到需要手术,这样不会伤害到眼睛。
- 在去除混浊晶状体后,眼科医生在其位置放置一个人工晶状体。人工晶状体是一个透明的镜片,不需要任何护理,成为眼睛的永久部分。
- 白内障手术后,大多数人需要阅读眼镜或远视。有一个相对较新的选择,多焦点眼内透镜,它们专注于同一透镜中的近距离和远距离。许多接受多焦点眼内透镜的人可能不需要戴眼镜。
家庭护理
对于早期白内障,可以通过使用不同的眼镜、放大镜或更强的照明来改善视力。如果这些措施没有帮助,或者如果视力障碍妨碍了每天的活动,比如开车、看书或看电视,手术是唯一有效的治疗方法。
预防
有助于减少白内障发生的方法,包括如下:- 在户外活动戴帽子,有紫外线防护的太阳镜。
- 管控好慢性疾病,如糖尿病、高血压等。
- 补充必要的维生素和抗氧化剂,可咨询医生。
- 定期检查眼睛。
参考文献:
1. Giblin FJ. Glutathione: a vital lens antioxidant. J Ocul Pharmacol Ther. 2000 Apr;16(2):121-35.
2. Kamei A. Glutathione levels of the human crystalline lens in aging and its antioxidant effect against the oxidation of lens proteins. Biol Pharm Bull. 1993 Sep;16(9):870-5.
3. Boscia F, Grattagliano I, Vendemiale G, Micelli-Ferrari T, Altomare E. Protein oxidation and lens opacity in humans." Investigative Ophthalmology and Visual Science. 2000;41(9):2461-2465.
4. Lou MF. Redox regulation in the lens. Progress in Retinal and Eye Research. 2003;22:657–682.
5. Xing KY et al. Effect of age on the thioltransferase (glutaredoxin) and thioredoxin systems in the human lens. Investigative Ophthalmology & Visual Science. 2010;51(12):6598–6604.
6. Spector A. Oxidative stress-induced cataract: mechanism of action. Federation of American Societies for Experimental Biology Journal. 1995;9(12):1173-1182.
7. Atkuri KR et al. N-Acetylcysteine--a safe antidote for cysteine/glutathione deficiency. Curr Opin Pharmacol. 2007 Aug;7(4):355-9.
8. Jariwalla RJ et al. Restoration of blood total glutathione status and lymphocyte function following alpha-lipoic acid supplementation in patients with HIV infection. Journal of alternative and complementary medicine (New York, N.Y.) Mar 2008;14(2):139-146.
9. Jiang X et al. [Effects of organic selenium supplement on glutathione peroxidase activities: a meta-analysis of randomized controlled trials]. Wei sheng yan jiu = Journal of hygiene research. Jan 2012;41(1):120-123.
10. Michael R et al. The ageing lens and cataract: a model of normal and pathological ageing. Philosophical Translations of the Royal Society B. 2011;366(1568):1278-1292.
11. Ravindran RD et al. Inverse association of vitamin C with cataract in older people in India. Ophthalmology. 2011 Oct;118(10):1958-1965.e2.
12. Jacques PF et al. Long-term vitamin C supplement use and prevalence of early age-related lens opacities. American Journal of Clinical Nutrition. 1997;66:911-916.
13. Tan AG et al. Antioxidant nutrient intake and the long-term incidence of age-related cataract: the Blue Mountains Eye Study. American Journal of Clinical Nutrition. 2008;87(6):1899-1905.
14. Simon JA et al. Serum ascorbic acid and other correlates of self-reported cataract among older Americans. Journal of Clinical Epidemiology. 1999;52(12):1207-1211.
15. Bunce GE. Nutritional factors in cataract. Annual Review of Nutrition. 1990;10:233-254.
16. Mares-Perlman JA et al. Diet and nuclear lens opacities. Am J Epidemiol. 1995 Feb 15;141(4):322-34.
17. Cumming RG et al. Diet and cataract: the Blue Mountains Eye Study. Ophthalmology. 2000 Mar;107(3):450-6.
18. Wang P et al. Hyperoxia-induced lens damage in rabbit: protective effects of N-acetylcysteine. Molecular Vision. 2009;15:2945-2952.
19. Pizzorno JN, Murray M Eds. Textbook of Natural Medicine, Second Edition.
20. Zafarullah M et al. Molecular mechanisms of N-acetylcysteine actions. Cellular and Molecular Life Sciences. 2003;60(1):6-20.
21. Radtke KK et al. Interaction of N-acetylcysteine and cysteine in human plasma. Journal of Pharmaceutical Sciences. 2012;101(12):4653-4659.
22. Zhao C et al. Prevention of acetaminophen-induced cataract by a combination of diallyl disulfide and N-acetylcysteine. Journal of Ocupational Pharmacology Therapy. 1998;14(4):345-355.
23. Carey JW et al. In vivo inhibition of l-buthionine-(S,R)-sulfoximine-induced cataracts by a novel antioxidant, N-acetylcysteine amide. Free Radic Biol Med. 2011 Mar 15;50(6):722-9.
24. Zhang S et al. Effects of N-acetylcysteine and glutathione ethyl ester drops on streptozotocin-induced diabetic cataract in rats. Molecular Vision. 2008 (14):862-870.
25. Packer L et al. Alpha-lipoic acid as a biological antioxidant. Free Radical Biology Medicine. 1995;19(2):227-250.
26. Maitra I et al. Stereospecific effects of R-lipoic acid on buthionine sulfoximine-induced cataract formation in newborn rats. Biochem Biophys Res Commun. 1996 Apr 16;221(2):422-9.
27. Kojima M et al. Efficacy of alpha-lipoic acid against diabetic cataract in rat. Jpn J Ophthalmol. 2007 Jan-Feb;51(1):10-3.
28. Bast A et al. Interplay between lipoic acid and glutathione in the protection against microsomal lipid peroxidation. Biochimica et Biophysica Acta. 1988 16;963(3):558-561.
29. Albanes D et al. Alpha-Tocopherol and beta-carotene supplements and lung cancer incidence in the alpha-tocopherol, beta-carotene cancer prevention study: effects of base-line characteristics and study compliance. Journal of the National Cancer Institute. 1996;88 :1560-1570.
30. Mayo Clinic. http://www.mayoclinic.com/health/vitamin-e/NS_patient-vitamine Last updated September 1 2012.
31. Christen WG et al. Vitamin E and age-related cataract in a randomized trial of women. Ophthalmology. 2008 May;115(5):822-829.e1.
32. Leske MC et al. Biochemical factors in the lens opacities. Case-control study. The Lens Opacities Case-Control Study Group. Arch Ophthalmol. 1995 Sep;113(9):1113-9.
33. Lyle BJ, Mares-Perlman JA, Klein BE, et al. Serum carotenoids and tocopherols and incidence of age-related nuclear cataract. American Journal of Clinical Nutrition. 1999;69(2):272-277.
34. Yaqci R et al. Use of melatonin to prevent selenite-induced cataract formation in rat eyes. Current Eye Research. 2006;31(10):845-850.
35. Taysi S et al. Melatonin reduces oxidative stress in the rat lens due to radiation-induced oxidative injury. Int J Radiat Biol. 2008 Oct;84(10):803-8.
36. Abe M et al. Inhibitory effect of melatonin on cataract formation in newborn rats: evidence for an antioxidative role for melatonin. J Pineal Res. 1994 Sep;17(2):94-100.
37. Arnal E et al. Lutein prevents cataract development and progression in diabetic rats. Graefe’s Archives in Clinical and Experimental Ophthalmology. 2009;247(1):115-120.
38. Gao S et al. Lutein and zeaxanthin supplementation reduces H2O2-induced oxidative damage in human lens epithelial cells. Molecular Vision. 2011(17):3180-3190.
39. Kijlstra A et al. Lutein: more than just a filter for blue light. Prog Retin Eye Res. 2012 Jul;31(4):303-15.
40. Chasan-Taber L et al. A prospective study of carotenoid and vitamin A intakes and risk of cataract extraction in US women. Am J Clin Nutr. 1999 Oct;70(4):509-16.
41. Vu HT et al. Lutein and zeaxanthin and the risk of cataract : the Melbourne visual impairment project. Investigative Ophthalmology & Visual Science. 2006;47(9):3783-3786.
42. Moeller SM et al. Associations between age-related nuclear cataract and lutein and zeaxanthin in the diet and serum in the Carotenoids in the Age-Related Eye Disease Study, an Ancillary Study of the Women's Health Initiative. Archives of ophthalmology. Mar 2008;126(3):354-364.
43. Olmedilla B et al. Lutein, but not alpha-tocopherol, supplementation improves visual function in patients with age-related cataracts: a 2-y double-blind, placebo-controlled pilot study. Nutrition (Burbank, Los Angeles County, Calif.). Jan 2003;19(1):21-24.
44. Tsuda T. Dietary anthocyanin-rich plants: biochemical basis and recent progress in health benefits studies. Molecular nutrition & food research. Jan 2012;56(1):159-170.
45. Karlsen A et al. Bilberry juice modulates plasma concentration of NF-kappaB related inflammatory markers in subjects at increased risk of CVD. Eur J Nutr. Sep 2010;49(6):345-355.
46. Miyake S, Takahashi N, Sasaki M, Kobayashi S, Tsubota K, Ozawa Y. Vision preservation during retinal inflammation by anthocyanin-rich bilberry extract: cellular and molecular mechanism. Lab Invest. 2012 Jan;92(1):102-9.
47. Fursova AZ et al. [Dietary supplementation with bilberry extract prevents macular degeneration and cataracts in senesce-accelerated OXYS rats]. Adv Gerontol. 2005;16:76-9.
48. Kawabata F et al. Effects of dietary supplementation with a combination of fish oil, bilberry extract, and lutein on subjective symptoms of asthenopia in humans. Biomedical research (Tokyo, Japan). Dec 2011;32(6):387-393.
49. Shim SH et al. Ginkgo biloba extract and bilberry anthocyanins improve visual function in patients with normal tension glaucoma. J Med Food. 2012 Sep;15(9):818-23.
50. Zhu X et al. Selenium supplementation can slow the development of naphthalene cataract. Current Eye Research. 2012;37:163-169.
51. Chada S et al. Post-transcriptional regulation of glutathione peroxidase gene expression by selenium in the HL-60 human myeloid cell line. Blood. 1989;74(7):2535-2541.
52. Baker RD et al. Selenium regulation of glutathione peroxidase in human hepatoma cell line Hep3B. Arch Biochem Biophys. 1993 Jul;304(1):53-7.
53. Booth SL. Vitamin K: food composition and dietary intakes. Food & Nutrition Research. 2012:56.
54. Murata M et al. The role of aldose reductase in sugar cataract formation: aldose reductase plays a key role in lens epithelial cell death (apoptosis). Chem Biol Interact. Jan 2001.130-132, 617-25.
55. Thiagarajan R et al. Vitamin K1 prevents diabetic cataract by inhibiting lens aldose reductase 2 (ALR2) activity. Scientific Reports. 2019 Oct 11;9(1):14684.
56. Sai Varsha MK et al. Inhibition of diabetic-cataract by vitamin K1 involves modulation of hyperglycemia-induced alterations to lens calcium homeostasis. Exp Eye Res. 2014;128, 73-82.
57. Camacho-Barcia ML et al. Association of Dietary Vitamin K1 Intake With the Incidence of Cataract Surgery in an Adult Mediterranean Population: A Secondary Analysis of a Randomized Clinical Trial. JAMA Ophthalmol, 2017;135, 657-661.
58. Hipkiss AR et al. Carnosine reacts with protein carbonyl groups: another possible role for the anti-ageing peptide? Biogerontology. 2000;1(3):217-223.
59. Babizhayev MA. Structural and functional properties, chaperone activity and posttranslational modifications of alpha-crystallin and its related subunits in the crystalline lens: N-acetylcarnosine, carnosine and carcinine act as alpha- crystallin/small heat shock protein enhancers in prevention and dissolution of cataract in ocular drug delivery formulations of novel therapeutic agents. Recent Patents on Drug Delivery & Formulation. 2012;6(2):107-148.
60. Wang AM et al. Use of carnosine as a natural anti-senescence drug for human beings. Biochemistry (Mosc). 2000;65(7):869-871.
61. Bellia F et al. Carnosinase levels in aging brain: redox state induction and cellular stress response. Antioxidants & Redox Signaling. 2009;11(11): 2759-2775.
62. Everaert I et al. Vegetarianism, female gender and increasing age, but not CNDP1 genotype, are associated with reduced muscle carnosine levels in humans. Amino Acids. 2011;40(4):1221-1229.
63. Babizhayev MA et al. N-Acetylcarnosine sustained drug delivery eye drops to control the signs of ageless vision: glare sensitivity, cataract amelioration and quality of vision currently available treatment for the challenging 50,000-patient population. Clinical Interventions in Aging. 2009;4:31-50.
64. Attanasio F et al. Protective effects of L- and D-carnosine on alpha-crystallin amyloid fibril formation: implications for cataract disease. Biochemistry. 2009;48(27):6522-6531.
65. Shi Q et al. Effect of a combination of carnosine and aspirin eye drops on streptozotocin – induced diabetic cataract in rat. Molecular Vision. 2009;15:2129-2138.
66. Williams DL et al. The effect of a topical antioxidant formulation including N-acetyl carnosine on canine cataract: a preliminary study. Veterinarian Ophthalmology. Sep-Oct 2006;9(5):311-316.
67. Quinn PJ et al. Carnosine: Its properties, functions and potential therapeutic applications. Molecular Aspects of Medicine. 1992;13(5):379-444.
68. Reuter SE et al. Carnitine and acylcarnitines: pharmacokinetic, pharmacological and clinical aspects. Clinical pharmacokinetics. Sep 1 2012;51(9):553-572.
69. AMR. Acetyl-L-carnitine. Monograph. Alternative medicine review: a journal of clinical therapeutic. Apr 2010;15(1):76-83.
70. Swamy-Mruthinti S et al. Acetyl-L-carnitine decreases glycation of lens proteins: in vitro studies. Experimental Eye Research. 1999;69(1):109-115.
71. Gawecki M et al. [Carnitine level in human lens and density of cataract]. Klinika oczna. 2004;106(3 Suppl):409-410.
72. Elanchezhian R et al. Acetyl-L-carnitine prevents selenite-induced cataractogenesis in an experimental animal model. Current Eye Research. 2007;32(11):961-71.
73. Elanchezhian R et al. Regulatory effect of acetyl-l-carnitine on expression of lenticular antioxidant and apoptotic genes in selenite-induced cataract. Chemico-biological interactions. Mar 30 2010;184(3):346-351.
74. Kocer I et al. The effect of L-carnitine in the prevention of ionizing radiation-induced cataracts: a rat model. Graefes Archives in Clinical and Experimental Ophthalmology. 2007;245(4):588-594.
75. Jain AK et al. Effect of high-glucose levels on protein oxidation in cultured lens cells, and in crystalline and albumin solution and its inhibition by vitamin B6 and N-acetylcysteine: its possible relevance to cataract formation in diabetes. Free Radical Biology and Medicine. 2002;15;33(12):1615-1621.
76. Padival S et al. Pyridoxamine inhibits maillard reactions in diabetic rat lenses. Ophthalmic Research. 2006;38(5):294-302.
77. Polizzi FC et al. Increased DNA-glycation in type 2 diabetic patients: the effect of thiamine and pyridoxine therapy. Experimental and clinical endocrinology & diabetes. Jun 2012;120(6):329-334.
78. Head KA. Natural therapies for ocular disorders, part two: Cataracts and glaucoma. Alternative Medicine Reviews. 2001;6(2):141-166.
79. Matsuda H et al. Structural requirements of flavonoids and related compounds for aldose reductase inhibitory activity. Chemical and Pharmaceutical Bulletin (Tokyo). 2002;50(6):788-795.
80. McLauchlan WR et al. Quercetin protects against hydrogen peroxide-induced cataract. Biochemical Society Transcations. 1997;25(4):S581.
81. Stefek M et al. Eye lens in aging and diabetes: effect of quercetin. Rejuvenation Research. 2011;14(5):525-534.
82. Ramana BV et al. Defensive role of quercetin against imbalances of calcium, sodium, and potassium in galactosemic cataract. Biological trace element research. Oct 2007;119(1):35-41.
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国眼科眼健康网
http://www.geteyesmart.org
美国国立卫生研究院公众健康网
www.medlienplus.gov
美国国立眼病研究所
http://www.nei.nih.gov
加拿大眼科学会
http://www.cos-sco.ca
其他参考文献:详见具体的综合干预方案
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

